|
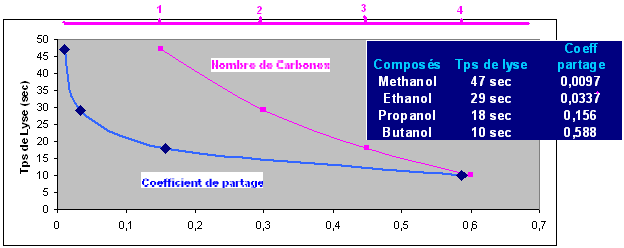
Résumé : Les globules rouges contenus dans le sang de lapin comme toutes les cellules animales ont une membrane très particulière et possédant de nombreuses propriétés. En effet elles sont semi perméable. Certaines substances pourront diffuser librement (eau, NO, CO2, O2, Urée) alors que dautres molécules, plus grosses ou polaires, ne pourront pas traverser la membrane.
Cette dernière permet de maintenir constante les concentrations intra et extracellulaires de divers ions (K+ et Na+). Dans le cas dun déséquilibre la cellule mourra (lyse). De part sa nature lipidique, la membrane sera plus perméable aux composés apolaires. Les molécules non diffusibles traverseront la membrane par des canaux spécifiques qui sont des protéines. Certains ions utilisent ces canaux pour diffuser dans le sens de leur gradient, mais des structures spécifiques sont nécessaires pour rétablir les concentrations ; ces pompes protéiques qui utilisent de lénergie sous forme d'ATP ne fonctionnent que dans certaines conditions
.
|