|
Glial cells generate neurons : the role of the transcription factor Pax6 |
Le gène Pax-6 (pour Paired box) est un facteur de transcription conservé au cours de lévolution, fortement exprimé dans loeil, et dont la fonction est requise pour la formation de cet organe. Cest le gène master dans le développement de lil de la drosophile. Grâce aux récents travaux de Nomura (2004), nous savons que Pax-6 joue également un rôle dans le développement du bulbe olfactif ainsi que dans la guidance et migration neuronale. Pax-6 code pour quatre protéines (p48, p46, p43 et p32/33).
Ce gène apparaît très tôt dans le neurectoderme et est essentiellement restreint à la région ventriculaire du tube neural constituée de progéniteurs neuraux en prolifération. Dans la région caudale du tube neural, future moelle épinière, la perte de fonction Pax6 affecte la différenciation de populations de neurones moteurs et d'interneurones.
Nous allons ici essayer de comprendre quel rôle joue Pax-6 dans la neurogenèse des cellules gliales.
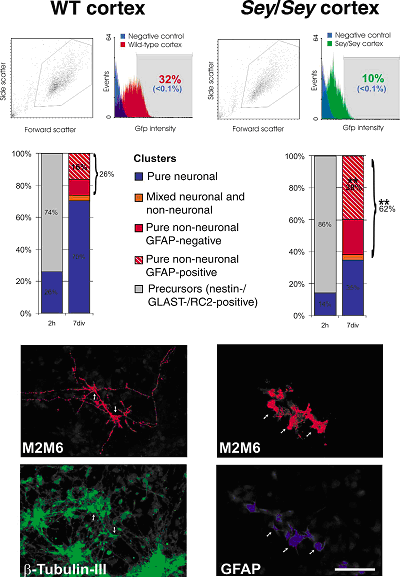
Lessentiel des méthodes sont basées sur la variation dexpression de Pax-6. Certaines manipulations viseront à ne pas exprimer Pax-6 (mutant sey / sey) et dautres dites de gain de fonction, sur-exprimant ce gène via laction dun rétrovirus sur des cellules in vitro
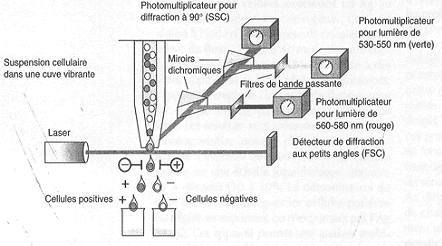
Cytométrie de flux ou FACS :La cytométrie de flux permet la numération des cellules exprimant un Antigène membranaire. La mesure du pourcentage de cellules est fonction de l'intensité de fluorescence liée aux Antigènes membranaires reconnus par des Anticorps spécifiques couplés à des fluorochromes. Ceci est réalisé à l'aide d'un analyseur de cellules : cytomètre de flux ou FACS (fluorescence activated cell sorter). Dans sa version sophistiquée, le cytomètre de flux permet aussi la séparation des cellules.


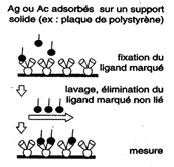
Les techniques d'immunomarquage, mettant en jeu les anticorps, sont parmi les plus performantes. Leur succès viens à la fois de leur facilité de mise en oeuvre, du nombres de molécules différentes que peuvent reconnaître les anticorps et du fait que les mêmes anticorps peuvent servir aussi bien à marquer des cellules en vue d'une observation microscopique qu'à des dosages extrèmement précis. Quand on arrive à trouver un anticorps qui reconnaît une molécule, le test est quasiment derrière. Ces possibilités et le fait qu'il est possible de produire quasiment n'importe quels anticorps à partir du moment où l'on dispose de la molécule à reconnaître ont fait qu'aujourd'hui, la plupart des tests diagnostics, dont celui du VIH dans le sang, sont basés sur les anticorps.
Il existe plusieurs techniques d'immunomarquage. L'immunohistofluorescence et l'immunihistochimie correspondent à l'immunomarquage des tissus biologiques, le premier utilisant un fluorophore comme marqueur alors pour le second c'est une enzyme. L'immunocytofluorescence et (beaucoup plus rarement) l'immunocytochimie correspondent au marquage de cellules ou d'organites cellulaires. Il existe aussi toutes les variantes utilisant la radioactivité et les métaux lourds pour le microscope électronique.
Les anticorpsLes anticorps sont des molécules complexes, appartenant à la famille des immunoglobulines (ce qui explique que l'abréviation courante d'anticorps soit Ig) communes à tous les vertébrés, elle même membre de la superfamille des immunoglobulines, qui comprend outre les immunoglobulines d'autres protéines apparentées qui possèdent souvent une fonction de reconnaissance. Ils sont fabriqués par les plasmocytes, des lymphocytes B activés. Les anticorps ont une seule fonction : reconnaître et se fixer de façon spécifique à une molécule nommée antigène. Les anticorps possédant deux sites de fixation pour cette molécule et chaque molécule possédant plusieurs zones de reconnaissance par les anticorps, cela entraîne une agglomération de la molécule et une précipitation qui l'inactive. Par ailleurs, les molécules marquées sont reconnues par les cellules immunitaires et détruites. Quand la molécule est portée par une bactérie, celle ci est tuée.
Les anticorps sont formés de deux chaînes lourdes et de deux légères assemblées pour former un Y. Ces chaînes sont réunies par des ponts disulfures très flexibles, par ailleurs la chaîne lourde est elle même articulée, l'ensemble est donc, malgré sa taille élevée, très déformable, ce qui est indispensable pour relier deux molécules qui n'ont pas forcement le bon goût d'être localisées à la bonne distance. Chaque chaîne est constituée d'une zone constante commune à tout les anticorps d'une même famille, et d'une zone variable, spécifique de chaque anticorps et qui reconnaît la molécule.
|
|
|
Le principe est extrêmement simple : la préparation qui comporte la molécule à mettre en évidence est plongée dans une solution contenant l'anticorps dit primaire. Celui ci se fixe de façon spécifique à l'antigène. Après rinçage, l'excès d'anticorps est évacué, il ne reste que celui qui s'est fixé. Cet anticorps pourrait être directement porteur du marqueur (fluorophore ou enzyme), toutefois, les biologistes ont choisi une deuxième solution : les anticorps produits par un animal sont eux même des antigènes pour un autre animal. Cet anticorps primaire va être à sont tour reconnu par un anticorps secondaire dirigé contre les anticorps de l'animal qui a servi à produire l'anticorps primaire et qui va réellement porter le marqueur. Il y a plusieurs avantages à l'utilisation d'une telle technique indirecte :
|
|
|
A l'heure actuelle, seuls les lymphocytes de vertébrés sont capables de produire des anticorps. Toutefois, au repos, l'animal produit peu d'anticorps. Pour qu'il produise les anticorps dirigés contre une molécule, il est nécessaire de la lui présenter. La première étape consiste donc à purifier cette molécule. Tant que cette première étape n'est pas achevée, il n'y a pas d'obtention d'anticorps possibles.
Les anticorps polyclonauxLes anticorps polyclonaux portent ce nom car ils sont produits par plusieurs clones de lymphocytes B. Les lymphocytes B ne sont capables de synthétiser qu'un seul anticorps. Le choix de cet anticorps est déterminé par des réarrangements chromosomiques effectués au hasard pendant l'hematopoiese. Chaque lymphocyte est donc virtuellement unique aux cellules résultant de sa propre division prés. Quand un lymphocyte B reconnaît l'antigène qui correspond à son anticorps, il va se diviser et les cellules filles vont se différencier en plasmocytes qui vont synthétiser l'anticorps. Les cellules filles résultant de la division d'un seul lymphocyte B sont appelées des clones.
L'antigène à reconnaître est injecté à l'animal. Il porte plusieurs épitopes, plusieurs lymphocytes B vont donc le reconnaître et se diviser. Après quelques semaines, une prise de sang va permettre récupérer le sérum contenant les anticorps synthétisés. Ils sont donc la production de plusieurs clones différents, d'où le nom de polyclonal.
La technique polyclonale présente un certain nombre d'inconvénient : le sérum contient des anticorps dirigés contre la protéine à reconnaître, mais aussi d'autres qui peuvent entraîner un parasitage du marquage. Par ailleurs, le type exact des anticorps produit par un lymphocyte est le fruit du hasard. D'un animal à l'autre les anticorps résultant par un même protocole d'immunisation peuvent être différents et les résultats être partiellement non reproductibles. Il n'est pas rare que la mort de l'animal entraîne la disparition d'un anticorps polyclonal très efficace dont aucun équivalent ne pourra être retrouvé plus tard. C'est pour ça que des animaux à durée de vie longue (cheval, chèvre, porc) sont couramment utilisés à coté des animaux plus traditionnels tels que le rat et la souris. De plus, la production du sérum par un seul animal limite sa diffusion. Enfin, la nécessité de prendre le sérum directement sur l'animal oblige à choisir des animaux de grande taille pour avoir une production suffisante. En revanche les anticorps polyclonaux ont extrement sensibles en raison du nombre important d'épitope reconnu sur un seul antigène.
Les anticorps monoclonauxIls résolvent les inconvénients des anticorps polyclonaux. Ils sont en effet fabriqué par un seul clone de lymphocyte B donc ils sont tous identiques et reconnaissant un seul épitope. Ils gagnent donc en précision ce qu'ils perdent en sensibilité. Ils sont en plus fabriqués par des cultures cellulaires, leur durée de production dépasse donc la vie de l'animal, elle est quasiment eternelle. De plus, des petits animaux peuvent être utilisés tels que les souris pour donner naissance aux lymphocytes, ce qui permet de tester un grand nombre d'anticorps pour trouver le bon.
La première étape est la production d'un sérum polyclonal par la méthode précédente. Les sérums sont testés pour trouver celui qui reconnaîtra le mieux la molécule. Quand on a ce sérum, on récupère les plasmocytes, certains sont présents dans le sérum avec les cellules sanguines, et on les met en culture dans des plaques à trou. Chaque puit de la plaque contient un nombre réduit de clone et donc un sous ensemble des anticorps du sérum total. La production de chaque puit est testée pour trouver celui qui produit le bon anticorps. A ce stade, les cellules sont normales, cela signifie qu'après quelques divisions les cellules vont vieillir et mourir. Il est nécessaire de les immortaliser pour obtenir une culture continue. On y arrive en les fusionnant avec des cellules de lymphome, donc déjà immortelles. On obtient des hybridomes qui vont avoir à la fois être limmortelle et produire des anticorps. Les cellules ininteressantes sont remisent en culture dans une plaque à puit à une dilution moyenne d'une seule cellule par puit. Le puit produisant le bon anticorps est recherché et a nouveau diluée de la même façon. A ce stade, chaque puit ne contient qu'un seul clone de cellule. Celui qui produit l'anticorps désiré peut alors être mis en culture en volumes plus important. Il synthétisera éternellement l'anticorps.
On peut noter que la molécule antigénique peut être mal purifiée. La phase de criblage des hybridomes va permettre d'isoler progressivement un clone producteur d'un anticorps spécifique de la molécule même si au départ le sérum reconnaît plusieurs protéines. L'anticorps produit va permettre en retour de purifier la protéine.
|
|
|
|
|
|
|
|
|
|
|
|
|
|
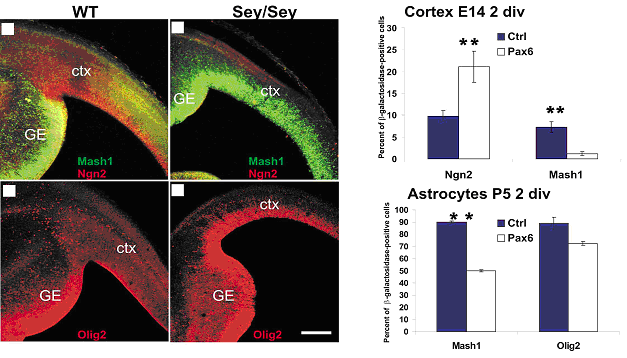
Analyse des cellules de E14 du cortex de souris sauvage et mutante sey / sey .
Le marquage de Ngn2 (neurogénine 2) est diminué chez les mutants, à linverse celui de Mash1 et Olig2 est augmenté.
Or la Ngn2 et Mash1 permettent aux cellules souches de se différencier en précurseurs neuronaux et Olig2 oriente la différentiation vers le phénotype glial.
(En effet Olig2 est connu pour jouer un rôle important dans linduction du caractère glial)
cette transcription cest le cas de la Ngn2 soit il la diminue cest le cas de Mash1 et Olig2
Discussions et Conclusion :
Lensemble des recherches permet de conclure que le facteur de transcription Pax6 est impliqué dans la neurogenèse des précurseurs de cellules gliales radiaires. On observe le même effet pour les astrocytes post-natal in vitro. Pax6 influence la transcription des gènes proneuraux, ce qui révèle au moins partiellement son mode daction. Il est donc très important au niveau des précurseurs neuronaux et des astrocytes. Ensuite nous avons vu que les cellules GFP négative nétaient pas touchées par labsence de Pax6. Enfin la transduction de Pax6 dans les astrocytes peut conduire à la mise en place de neurones ceci peut être une avancée historique dans la possibilité de « régénérer les neurones ».